tRNA工学 × 放線菌酵素を利用した新しい抗生物質創出法の開発
■ 概要
細菌感染症の治療に不可欠な抗生物質は、現代医療を支える重要な医薬品です。しかし近年、既存薬が効きにくい多剤耐性菌の増加が世界的な問題となっており、新しい作用や構造をもつ抗生物質の創出が強く求められています。富山大学・和漢医薬学総合研究所の森田洋行教授らの研究グループは、東京大学や北海道大学などの研究グループとともに、福井県立大学生物資源学部の丸山千登勢准教授、濱野吉十教授らが主導する共同研究に参画し、放線菌が生産する強い抗菌作用をもつ抗生物質「ストレプトスリシン(ST)」の分子構造を人工的に改変できる新たな手法の開発に成功しました。森田教授らの研究グループは、この共同研究において、主として酵素の立体構造解析を主に担当しました。本研究では、ST類抗生物質の分子構造を改変するケモエンザイマティック手法の開発に貢献し、これまでにない新規ST誘導体を多数創製することに成功しました。本成果は、tRNAを利用した天然物改変という新しい分子設計戦略を提示するものであり、抗生物質をはじめとするペプチド系天然物の化学多様性拡張に大きく貢献します。将来的には、新規抗生物質の開発を加速し、感染症治療に新たな道を切り開くことが期待されます。
本研究成果は、米国化学会誌「Journal of the American Chemical Society」に2026年3月13日(金)(日本時間)に掲載されました。
■研究の背景
微生物は多様なペプチド性天然物を生産しており、これらは医薬品シーズとして重要な役割を果たしています。一般に、ペプチド骨格はリボソーム、非リボソーム型ペプチド合成酵素(NRPS)、あるいはATP-grasp酵素によって構築されます。特にNRPSやATP-grasp系では非天然型アミノ酸も取り込まれるため、化学構造の多様性が大きく拡張されます。一方で、リボソーム依存型の生合成では、tRNAに結合したタンパク質性アミノ酸のみが利用されるため、構造多様性は限定的であると考えられてきました。しかし近年、アミノアシルtRNAはタンパク質合成以外にも、細胞壁生合成や天然物生合成など、さまざまな生化学反応に関与することが明らかになりつつあります。
ストレプトスリシン系抗生物質は、多剤耐性菌に対する有効性が期待される化合物群であり、その抗菌活性や選択毒性は、コア構造に結合するアミノアシル側鎖の違いに強く依存しています。これまでの研究から、β-リシン側鎖はNRPSによって導入される一方、グリシン側鎖はFemX様酵素Orf11により、アミノアシルtRNAを利用して導入されることが明らかになっています。しかし、これらの酵素はいずれも高い基質特異性を示すため、天然には限られた側鎖構造しか存在しません。そのため、より多様な誘導体を創出するには、基質許容性を有する酵素の探索と、その分子機構の理解が重要な課題となっていました。
このような背景から、本研究では、基質許容性を有するtRNA依存型アミド結合形成酵素に着目しました。複数のアミノアシルtRNAを受け入れる酵素と、特定の基質に特異的な近縁酵素を比較解析することで、基質認識機構の解明とともに、アミノアシル側鎖構造を自在に改変可能なケモエンザイマティック手法の確立が期待されます。
■研究の内容・成果
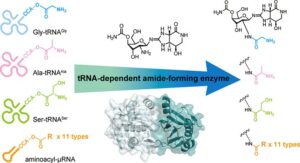
本研究では、ストレプトスリシン抗生物質の側鎖構造を改変する新たな手法として、tRNA依存型アミド結合形成酵素Sba18を利用したケモエンザイマティック手法を開発しました。Sba18は、従来知られていたGly特異的酵素とは異なり、Gly-tRNAに加えてAla-tRNAおよびSer-tRNAも基質として受け入れることが可能であり、実際に新規誘導体であるアラニルスリシンおよびセリルスリシンの生成に成功しました。
さらに、フレキシザイム技術を用いて人工的に調製した多様なアミノアシルtRNA類似体を基質として用いることで、合計13種類の新規ストレプトスリシン誘導体の創出を達成しました。生成された化合物の生物活性評価の結果、アラニルスリシンは抗菌活性を保持しつつ真核微生物に対する活性を示さないことが明らかとなり、側鎖構造の改変によって選択的毒性を制御できる可能性が示されました。
また、Sba18およびその近縁酵素Sbb17のX線結晶構造解析を行い、両酵素の比較により基質認識機構を分子レベルで解明しました。両者は全体構造および触媒中心を共有する一方で、Sbb17がグリシンに特異的であるのに対し、Sba18はより広い基質許容性を示すことが明らかとなりました。さらに、キメラ酵素および部位特異的変異解析により、基質特異性の違いは酵素中部領域の特定のアミノ酸残基(117位および178位)に起因することを突き止めました。
これらの成果は、アミノアシルtRNA依存型酵素の基質認識機構の理解を大きく前進させるとともに、抗生物質をはじめとするペプチド天然物の構造多様化を可能にする分子基盤を提供するものです。本手法は非天然基質の導入にも適用可能であり、新規創薬シードの創出に向けた有力な戦略として期待されます。
■今後の展開
細菌感染症の治療に不可欠な抗生物質は、現代医療を支える重要な医薬品です。しかし近年は、既存薬が効きにくい「薬剤耐性菌」が世界的に増え、大きな社会問題となっており、新しい作用や構造をもつ抗生物質の創出が強く求められています。本研究成果は、将来の新しい抗生物質の開発につながる可能性があり、感染症治療の新たな道を切り開くものと期待されます。
【論文詳細】
論文名:
tRNA-dependent chemoenzymatic transformation of aminoacyl pendant moieties of streptothricin antibiotics
著者:
丸山千登勢,中嶋優,松田貫暉,Sherif A. Hamdy,内山駿,後藤佑樹,森貴裕,小笠原泰志,新家一男,阿部郁朗,大利徹,菅裕明,森田洋行,濱野 吉十
掲載誌:
Journal of the American Chemical Society (2026年3月13日オンライン掲載)
DOI:
2026.04.03 研究成果









